Propiedades del Tabla Periódica: Una Mirada en Profundidad
La tabla periódica de los elementos es uno de los logros más importantes de la ciencia moderna. Desarrollada en su forma contemporánea por Dmitri Mendeléyev en 1869, esta herramienta no solo organiza los elementos químicos de manera sistemática, sino que también proporciona un marco para entender sus propiedades, comportamientos y relaciones entre sí. En este artículo, exploraremos en profundidad las propiedades de la tabla periódica, su estructura, y cómo estas propiedades influyen en la química y la vida cotidiana.
La Estructura de la Tabla Periódica
La tabla periódica está compuesta por filas horizontales llamadas periodos y columnas verticales llamadas grupos o familias. Cada elemento en la tabla está representado por su símbolo químico, número atómico y, en algunos casos, su masa atómica. A continuación, se detallan las características fundamentales de la estructura de la tabla.
Periodos
Los periodos representan el número de capas de electrones en un átomo. A medida que se desciende en la tabla, los elementos del mismo periodo tienen el mismo número de niveles de energía, pero el número de electrones y protones aumenta. Por ejemplo, los elementos del primer periodo (hidrógeno y helio) tienen un solo nivel de energía, mientras que los del segundo periodo tienen dos.
Grupos
Los grupos, o familias, contienen elementos que comparten propiedades químicas y físicas similares debido a la configuración de electrones en su capa externa. Los elementos en el grupo 1 son metales alcalinos, conocidos por su alta reactividad, mientras que los del grupo 18 son gases nobles, que son notablemente inertes.
Propiedades Periódicas
Existen varias propiedades que cambian de manera predecible a lo largo de la tabla periódica. Estas incluyen la electronegatividad, la energía de ionización, el radio atómico y la reactividad.
Electronegatividad
La electronegatividad se refiere a la tendencia de un átomo a atraer electrones hacia sí mismo en un enlace químico. Esta propiedad aumenta de izquierda a derecha a lo largo de un periodo y disminuye al descender en un grupo. Por ejemplo, el flúor es el elemento más electronegativo, mientras que el cesio es uno de los menos electronegativos. Esta tendencia se puede atribuir a la mayor carga nuclear efectiva que experimentan los electrones en la misma capa de valencia a medida que se añaden más protones en el núcleo.
Energía de Ionización
La energía de ionización es la cantidad de energía necesaria para eliminar un electrón de un átomo en estado gaseoso. Al igual que la electronegatividad, la energía de ionización tiende a aumentar de izquierda a derecha y disminuir al bajar en un grupo. Los metales, que se encuentran a la izquierda de la tabla, generalmente tienen energías de ionización más bajas, lo que los hace más propensos a perder electrones y formar iones positivos.
Radio Atómico
El radio atómico se define como la distancia desde el núcleo de un átomo hasta el límite de su nube de electrones. A medida que se avanza hacia la derecha en un periodo, el radio atómico disminuye debido a la mayor atracción entre el núcleo cargado positivamente y los electrones en la misma capa. En contraste, al descender en un grupo, el radio atómico aumenta, ya que se añaden capas de electrones adicionales.
Reactividad
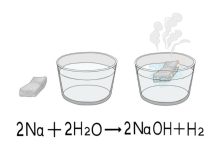
La reactividad de los elementos varía significativamente a lo largo de la tabla periódica. Los metales alcalinos son extremadamente reactivos, especialmente el litio, el sodio y el potasio, que reaccionan violentamente con el agua. Por otro lado, los gases nobles, ubicados en el grupo 18, son prácticamente no reactivos debido a su configuración electrónica completa.
Importancia de la Tabla Periódica
La tabla periódica no solo es una herramienta de referencia para los químicos, sino que también tiene aplicaciones en otras disciplinas científicas, como la biología, la física y la ingeniería. Conocer las propiedades periódicas permite predecir comportamientos de reacciones químicas, formular nuevos compuestos y entender mejor los procesos biológicos que dependen de la química.
Aplicaciones Prácticas
Las propiedades de los elementos y su organización en la tabla periódica tienen un impacto directo en muchas áreas de la vida diaria. Por ejemplo, en la medicina, el conocimiento de la química de los elementos permite el desarrollo de fármacos y tratamientos. En la industria, la selección de materiales para la construcción, la electrónica y la manufactura depende de las propiedades de los elementos.
Conclusiones
La tabla periódica es mucho más que una simple lista de elementos. Es una representación visual y conceptual de las relaciones y propiedades que rigen la materia. A través del estudio de sus propiedades periódicas, los científicos pueden desentrañar los secretos del mundo químico, contribuyendo al avance del conocimiento humano. Su estructura, que permite una organización lógica y predecible, es fundamental para la comprensión de la química y sus aplicaciones en la vida cotidiana.
Referencias
- Atkins, P. W. (2010). Physical Chemistry. Oxford University Press.
- Chang, R. (2010). Chemistry. McGraw-Hill.
- Zumdahl, S. S. (2013). Chemistry. Cengage Learning.
Con esta base de conocimiento sobre la tabla periódica, podemos apreciar su relevancia no solo en el ámbito científico, sino también en su aplicación práctica en diversos campos. La comprensión de las propiedades de los elementos es esencial para el progreso en la química y sus múltiples aplicaciones en nuestra vida diaria.